新型コロナウイルス感染症(COVID-19)による経済への影響が世界的に深刻さを増す中、到来が確実視される第2波、第3波に対する懸念が高まっている。感染終息にはワクチンの迅速な開発と供給が欠かせない。世界保健機関(WHO)によると5月22日現在すでに123のワクチン開発の計画が進行中で(注1)、国際的な開発競争の様相を呈している。特許による開発成果の専有化を防ぐため特許に制限をかける流れになりつつあるが、開発インセンティブを損なう恐れも危惧される。本稿では、ワクチン開発のインセンティブとアクセスを両立するための国際的な枠組みについて考えてみたい。
COVID-19ワクチンには特許が適用されない可能性も
5月18-19日に開催されたWHO総会では、米中対立を受けてWHOの対応をめぐる検証に注目が集まったが、今後のワクチン開発と供給に影響を与えうる重要な指針が示された。総会ではCOVID-19の制圧に必要な技術知識や製品、それらを構成する部分品や必要な設備への公平かつ手頃な価格でのアクセスを確保するためその障害を取り除くことに向けて国際協調を目指す決議が採択された(注2)。利害関係者には治療薬やワクチンのタイムリーかつ手頃な価格でのアクセスを確保するため、既存のパテントプールを活用し自発的な共有やライセンスを呼び掛けている(注3)。さらに同決議の中では、こうした方針が、医薬品の特許保護を定めた世界貿易機関(WTO)「知的所有権の貿易関連の側面(TRIPS協定)」とその柔軟性規定とされる2001年「TRIPS協定と公衆衛生に関する特別宣言(ドーハ宣言)」の考え方と整合性を持つことが記されている。
ドーハ宣言は、TRIPS協定に規定のあった国家的緊急事態下では特許権者の許諾を得ずに技術を使用できる強制実施権の発動条件に、HIV/エイズ・結核・マラリアなどの感染症の蔓延が含まれると明記した。この背景には特許保護によって薬価が高額になり発展途上国の患者が薬にアクセスできない問題があった。これにより国内に生産能力のある途上国は、感染症を理由に強制実施権を発動し、特許薬を国内で生産できるようになった。強制実施権発動による生産は国内向けにのみ認められていたが、2003年には、国内に生産能力がない国に対して輸出を認める方針も示され、2017年にTRIPS協定の初改正として恒久的に定められた。実際に、強制実施権はブラジル、インド、インドネシア、タイ、マレーシア、モザンビーク、ジンバブエなどで発動された事例があり、輸出についてもカナダがルワンダに対して抗HIV薬の製造・輸出を行った事例がある。COVID-19に関しては、すでに今年の3月にイスラエルが強制実施権を発動しており、インドで生産された抗HIV薬カレトラの後発品の輸入に踏み切っている。WHO総会で示されたTRIPS協定の柔軟性規定との整合性は、将来ワクチンが開発された際にアクセスに窮する恐れがある国々には朗報だったに違いない。
COVID-19ワクチンは“グローバル公共財”
同決議ではCOVID-19ワクチンの広範な接種を“グローバル公共財(a global public good for health)”と表現しているが、実際のところ世界的に蔓延する感染症ワクチンを開発し広範な接種を実現していくことは経済学的にもグローバル公共財の要件を満たす(Kremer, 2000a)。ある人がワクチンを服用することは、本人の感染確率を下げるとともに、服用していない他人の感染確率を下げるという利益(外部経済効果)を与える。これは摂取していない人も予防効果を同時に享受できるという点で公共財の非競合性(同時に複数が消費可能)に該当する。さらに、ワクチンを接種せずに他人の接種にタダ乗りする人を排除できないという点で公共財の非排除性(費用を払わずに利用している人を排除できない)にも該当する。従って消費者は可能ならばワクチンを購入せずに他人のワクチン摂取にタダ乗りしようと考えることから、放置すればワクチン需要は小さくなり、開発者はワクチンを開発するインセンティブを持たなくなる。従って、ワクチンは過小供給に陥りやすく、集団予防接種の実施や国公立研究機関等が開発を担うなど、もともと公的な介入が必要とされる分野である。COVID-19はスペイン風邪以来の世界的流行であり、グローバル化の進展により国境を超えた伝播も極めて早い。上記の公共財の要件で示した例を“人”でなく“国”に置き換えると、COVID-19ワクチンの開発・接種は世界が強調して取り組むべきグローバル公共財と考えることができる。
公共財だが開発の主役は民間の製薬会社
ワクチンに公共財の性質があることを勘案すると、民間よりも公的機関が開発に積極的であると考えられる。しかし、5月22日時点のCOVID-19候補ワクチン123事例を筆者が調査したところ、公的機関(政府系機関・非営利・大学等)は38(30.9%)、製薬会社と公的機関の共同開発が28(22.8%)、製薬会社は57(46.3%)となり、製薬会社の存在が際立つ結果となっている(図1)。臨床評価の段階に入っている10件に限ってもうち6件が製薬会社で残りの4件についても公的機関との共同開発である。国籍別に見るとやはり米国が占める割合が突出して高い(図2)(注4)。米国単独が25件、複数国の共同開発23件のうち17件には米国の開発主体が参画している。
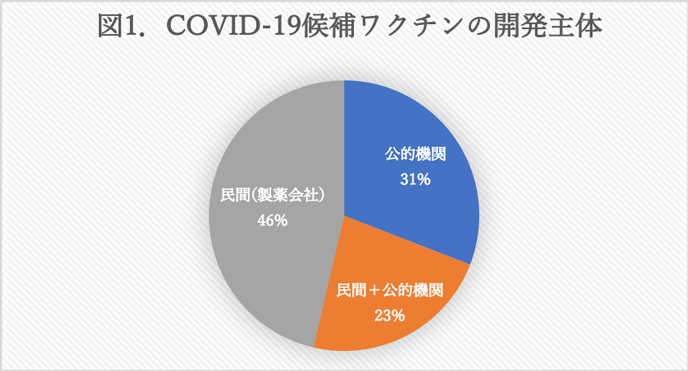
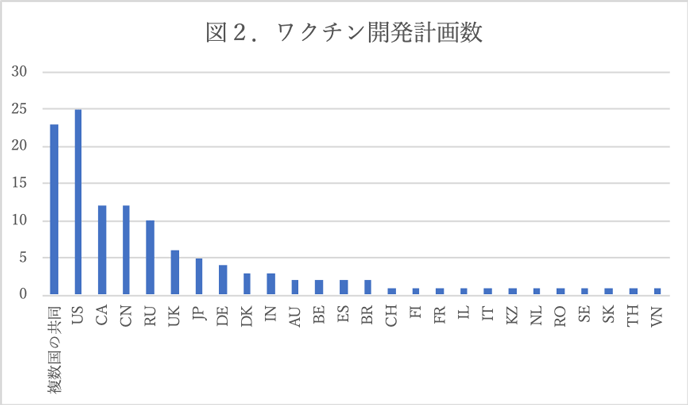
民間の開発割合が高い傾向はHIV/エイズ・結核・マラリアについても見られ(伊藤,2005)、製薬会社が公的機関よりも研究開発をリードしている。三大感染症向け医薬品の特許出願人の情報からどのような企業属性を持つのか検証したところ、研究開発ストック規模の大きい大手製薬会社や、さまざまな疾病分野をカバーしている製薬会社ほど感染症向け医薬品開発で優位性を持っている(伊藤・山形, 2004)。医薬品開発の場合、範囲の経済性ともいうべき効果が開発を有利にする可能性がある。実際にCOVID-19の治療薬でも類似性などから他の疾病向けの薬を試す例が数多く報告されており、感染症に限らず幅広い疾病から多くの知見が得られているようだ。
開発インセンティブとアクセスを両立させる国際枠組みが必要
製薬会社の果たす役割が大きいことを考慮すると、強制実施権が濫用されると、医薬品開発のインセンティブを損なう恐れがある。たとえ特許権が認められたとしても国際世論から糾弾されるのを恐れ権利を放棄するかもしれない。実際に先述のイスラエルが発動した事例では、特許を保有する米国AbbVie社が3月に特許権を行使しないことを発表している。特許の不適用や自発的な放棄はワクチンの普及につながると期待されるが、将来の開発インセンティブを削ぐ恐れもあり、特許に替わる報奨システムも併せて議論すべきだ。
報奨には、補助金支給による事前的な政策と、特許制度によって独占権を付与するといったように事後的に報いる政策がある。事前的な政策では情報の非対称性により開発者が成功確率を過大評価したり、適切に資金が使われないなど開発努力を怠る恐れがある。一方、事後的な政策では、開発後、公共の利益を口実に約束した側が報奨を履行しないという時間的不整合の問題がある(注5)。日本政府は4月30日のG7財務大臣会合で、開発に成功した製薬会社から特許を買い取り、発展途上国を含む各国に安価に供給する仕組みを提案した。買取価格の決定方法(注6)や時間的不整合など課題もあるが、既存のパテントプールの活用と併せて、開発インセンティブとアクセスを両立させる国際的な仕組みを検討することは将来のパンデミックに対処するためにも重要な取り組みだ。
開発インセンティブとアクセスの両立はHIV/エイズ・結核・マラリアの三大感染症をはじめ発展途上国で蔓延するいわゆる“顧みられない病気(neglected tropical diseases)”(注7)も同じ課題を抱えている。世界の年間死者数はWHOの推計でHIV/エイズは77万人(2018年)、結核は124万人(2018年)、マラリアは43.5万人(2017年)(注8)にも上るが、感染が発展途上国に集中しており市場規模は必ずしも大きくない。開発インセンティブと薬へのアクセスを確保するためパテントプールや基金設立による薬の買い上げ(注9)などが実現されてきた。これにより薬へのアクセスは改善されたが、有効なHIVワクチンやマラリアワクチンは依然として未開発である。一方COVID-19は先進国で猛威を振るったことで未だかつてないスピードでワクチン開発が進んでいる。早期のワクチン開発による感染終息を願うと共に、これを機に開発インセンティブとアクセスを両立させる国際枠組みが構築され、他の深刻な感染症にも適用されることを期待したい。


