1.はじめに
新型コロナウイルス禍を機に製薬企業の新薬開発に対する関心は高まっている。新型コロナウイルスに対するワクチンは、2023年ノーベル生理学・医学賞の対象となったペンシルベニア大学発のmRNA安定化技術をモデルナおよびファイザーといった製薬企業が取り込み、いち早くワクチンの実用化にたどり着いた。
医薬品開発の主体は、1980年、1990年代の低分子化合物から、近年はバイオ医薬品などの高分子に移行し、さらに再生医療、遺伝子治療など、創薬モダリティ(注1)が多様化・複雑化している。新しい創薬モダリティは、業界の動向を変える「ゲームチェンジャー」となり得る。上述のmRNAも新しい創薬モダリティの1つであり、アカデミアやベンチャーの有する創薬シーズを製薬企業が開発につなげることに成功した事例であり、感染症以外にも、がんの治療などへの応用が期待されている。
一方で、日経新聞の記事(注2)(2022年6月)によると、製薬大手25社を対象に、実用化に近づいた候補品について10年前からの増減数を比較した結果、欧米大手が上位を席巻し、日本勢との差が鮮明になっている(表1)。
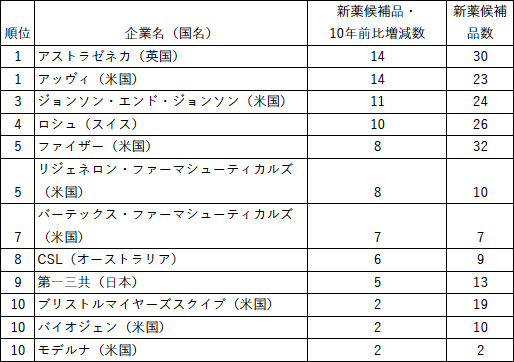
新しい創薬モダリティを生み出すアカデミアやベンチャーの研究力、および、それを取り込み実用化を目指す製薬企業の開発力が、新薬を生み出すファクターとなる流れは今後も変わらない。そこで、われわれは今後注目される新しい創薬モダリティの候補とその研究開発段階について調査した。
2.調査方法
まず学術文献レベルでどのような創薬モダリティが議論されているのかを把握するために、Elsevier Scopusデータから2019~2023年に新しい創薬モダリティに関して記載されている約280のレビューを抽出した。
次に、当該レビューの要約部分について、TextRankパッケージ(注3)により、単語が互いに続いているかどうかを確認して単語のネットワークを構築、そのネットワーク上でGoogle Pagerankアルゴリズムを適用して関連する単語を抽出し、互いに続いている関連する単語を組み合わせてキーワードを取得した。今回は名詞または形容詞のみを対象とした。
これら抜き出されたキーワードから、9つの新しい創薬モダリティ候補を特定した。
次に、特許データベースであるLexisNexis® PatentSight®を用いて、特許公報のうち「タイトル」、「要約」、または「特許請求の範囲」に上記創薬モダリティ候補に関連するキーワードを含む特許を抽出し、Patent Asset Index(注4)の高い特許出願人を調べた。
3.結果
近年、学術文献レベルで議論されている新しい創薬モダリティについて、9つの基盤技術が特定された。その概要を表2に示す(まだ用語が確立されていない分野もあるので、各創薬モダリティの候補名は筆者が独自に作成した点を留意いただきたい)。特に、mRNA医薬および再生医療・幹細胞の分野は、それぞれ2023年、2012年のノーベル生理学・医学賞の受賞対象となった分野である。

次に、当該9つの創薬モダリティについて、関連するキーワードが特許公報の「タイトル」、「要約」、または「特許請求の範囲」に記載されている特許を抽出し、Patent Asset Indexの高い特許出願人を調べた。
詳細は割愛するが、残念ながら今回の調査では日本の企業・大学等が上位に入る分野は存在せず、全ての分野において欧米の企業・大学等が上位を席巻し、中国の大学も上位に入る結果であった。唯一、再生医療・幹細胞の分野で、京都大学、大阪大学、および富士フイルムといった日本の企業・大学がランクインしている。
ここでは、各分野で大学や研究機関が占める割合に着目したい。国籍を問わず上位20および50に入る大学・研究機関の割合を示したのが表3である。
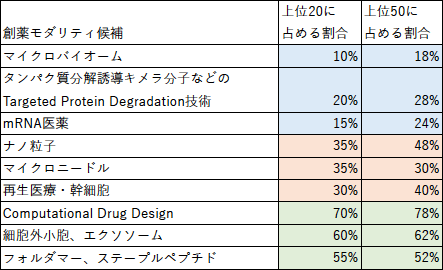
大学・研究機関の割合が低い(企業が占める割合が高い)場合、その創薬モダリティは応用段階に入っているものといえる。一方で、大学・研究機関の割合が高い場合、その創薬モダリティはまだ基礎研究の段階にあるものといえる。表3の通り、9つの創薬モダリティは3つの段階に分けられ、青色(大学・研究機関の割合が低い)のマイクロバイオーム、Targeted Protein Degradation技術、mRNA医薬はすでに応用段階に入っている可能性が高い。赤色(大学・研究機関の割合と企業の割合が同程度)のナノ粒子、マイクロニードル、再生医療・幹細胞は、基礎から応用段階への過渡期で、緑色(大学・研究機関の割合が高い)のデジタルを活用した新薬開発支援システム、細胞外小胞・エクソソーム、フォルダマー・ステープルペプチドは、基礎研究の段階といえる。
上述の通り、新型コロナウイルスに対するワクチンに関しては、大学発のmRNA安定化技術を製薬企業が取り込み、いち早くワクチンの実用化にたどり着いた。残念ながら、今回の手法で同定できた9つの基盤技術において、現時点では日本の大学・企業のプレゼンスは決して高いものではない。しかしながら、表3の赤色部分や特に緑色部分の創薬モダリティに関しては、まだまだ基礎研究の段階であり、十分に挽回できる時間的余地はある。国内外の大学発の技術を取り込むなどして、大学と企業の連携を深めることにより、わが国発の創薬も期待できるのではないか。



